شهیدان زنده اند
تبلیغشهیدان زنده اند
تبلیغحیاتی ترین نگهبان بدن خود را بهتر بشناسیم
نام P53 برگرفته از توده مولکولی آن می باشد که روی SDS-PAGE (سدیم دو دسیل سولفات پلی آکریل آمید ژل الکتروفورز ) به صورت یک پروتئین 53 کیلو دالتونی جدا می شود. اما اگر بر اساس تعداد اسیدهای آمینه آن شناسایی صورت بگیرد 43.7 کیلو دالتون خواهد بود این تفاوت به دلیل تعداد زیادی اسیدهای آمینه اطراف مولکول آن میباشد که در حرکت الکتروفورتیک سنگین تر از حالت طبیعی خود را نشان می دهد. این حالت در P53 گونه های مختلف شامل انسان ، جوندگان، قورباغه و ماهیها دیده می شود.
عملکرد P53:
P53 دارای مکانیسمهای ضد سرطانی زیادی
می باشد همچنین در آپپتوز، در پایداری ژنوم و جلوگیری از فعالیتهای رگزایی نقش
دارد. به عنوان عملکرد ضد سرطانی از مکانیسم های زیر استفاده می کند:
1 -
میتواند پروتئینهای ترمیم کنندهْ DNA را در مواردی که DNA
آسیب دیده تشخیص داده می شود فعال
نماید.
-2 با متوقف کردن چرخهْ سلولی در نقطهْ G1/S مانع رشد سلول شده تا آسیب تشخیص داده شده روی DNA ترمیم شود، بعد از ترمیم آسیب، مهارسلول برداشته می شود و سلول ادامهْ چرخهْ خود را انجام می دهد.
-3 آپپتوز را میتواند شروع نماید، آپپتوز مرگ برنامه ریزی شدهْ سلول است در حالتیکه آسیب DNA غیر قابل ترمیم باشد آپپتوز شروع خواهد شد.
مکانیسم عملکرد به این صورت است:
در حالت طبیعی P53 به مولکول mdm2 متصل بوده و غیر فعال می باشد به محض ایجاد آسیب DNA یا استرسهای سلولی دو حالت اتفاق می افتد.
الف: مهار P53 برداشته می شود و P53 فعال می گردد.
ب: میزان تولید P53 در سلول افزایش می یابد.
P53 فعال شده بهDNA وصل می شودو
باعث افزایش بیان چند ژن شامل WAF1/CIP1 می شود که مولکول P21 را کد می کنند.
P21 در فاز G1/S به CDK2 (Cycling Depended Kinas 2) متصل می شود و باعث مهار آن می گردد.
کمپلکس CDK2 برای ادامهْ
روند چرخهْ سلولی بسیار مهم می باشد و وقتی که P21 به آن متصل شد سلول نمی تواند وارد مرحلهْ بعدی تقسیم خود شود .
P53 جهش یافته نمی تواند برای مدت
طولانی به DNA وصل شود و در
نتیجه P21 نیز به مقدار
کافی در دسترس نخواهد بود تا سیگنال توقف تقسیم سلولی را ایجاد نماید، سلول به
صورت غیر قابل کنترل تقسیم خواهد شد و نتیجهْ آن ایجاد تومور خواهد بود. تحقیقات
اخیر اتصال مولکول P53 را به مولکول
دیگری بنام RB1 از طریق واسطه
ای بنام 14 P جهت مهار سیکل
سلولی نشان داده است.
بیانP53 را میتوان
به وسیلهْ قرار دادن سلول در معرض اشعهْ UV بررسی نمود. در این حالت اشعهْ UV باعث آسیب DNA شده و مقدار p53 در سلول افزایش می یابد.
تفاوت ساختار مغز محافظهکاران و لیبرالهای ایالات متحده
تفاوت ساختار مغز محافظهکاران و لیبرالهای ایالات متحده: دیدگاهی عصبشناختی

پژوهشها نشان میدهد محافظهکاران و لیبرالها نه تنها متفاوت رأی میدهند بلکه ساختار مغز آنان نیز با هم تفاوتهایی دارد. امروزه تحقیقات در روانشناسی سیاسی سبب پدیدآمدن عنوانی به نام نوروساینس سیاسی یا نوروپلیتیک (Neuropoltics) شدهاست. هدف از نوروپلیتیک، گردآوری و یکپارچهسازی نظریات و روشها به منظور بررسی مکانیسمهای شناختی عصبی در شناخت و رفتار سیاسی است.
چندی پیش مطالبی را در حوزه عصبشناختی و گرایشهای سیاسی مطالعه کردم که برایم جالب بود. پیرو صحبتهای دکتر محسن رنانی در باب انتخابات و اهمیت پرهیز از اختلافات سیاسی و همچنین نزاع بیپایان و بینتیجه اصولگرایان و اصلاحطلبان در مباحث گوناگون اجتماعی و سیاسی، به نظرم مناسب رسید مطالب خواندهشده پیشین را با دیگران به اشتراک بگذارم. مطلب زیر ترجمه خلاصه چندین کار پژوهشی انجامیافته در حوزه تفاوتهای عصبشناختی جمهوریخواهان و دموکراتها در آمریکا است. محافظهکاران و لیبرالها جدا از تفاوتهای مسلکی در زمینه دیگری هم با هم فرق دارند: عصبشناختی.
شانزده مطالعه علمی رفتاری و عصبشناسانه گردآوری شده و با بررسی آنها به این نتیجه میرسیم که [در ایالات متحده] تفاوتهای میان جمهوریخواهان [محافظهکار] و دموکراتها (لیبرال / آزادیخواه] بیشتر از تفاوتهای سطحی است. به گفته استیون مارکاف، "اصولاً، برای هزارهها طرفهای مختلف داشتهاند سر هم داد میکشیده اند، و ما میخواهیم دریابیم که علت ریشهای این در کجا میتواند باشد." افرادی که گرایشهای سیاسی یکسانی دارند چه نقاط مشترک دیگری با هم دارند؟ آیا تنها حس همدردی و همدلی، هواداران یک نامزد انتخاباتی را گردهم میآورد؟ آیا گرایشات سیاسی افراد میتواند منشاء ژنتیکی داشتهباشد؟ اساساً واکنش به انتخاب یک نامزد سیاسی "عاطفی" است یا "عقلانی"؟
پژوهشها نشان میدهد محافظهکاران و لیبرالها نه تنها متفاوت رأی میدهند بلکه ساختار مغز آنان نیز با هم تفاوتهایی دارد. امروزه تحقیقات در روانشناسی سیاسی سبب پدیدآمدن عنوانی به نام نوروساینس سیاسی یا نوروپلیتیک(Neuropoltics) شدهاست. هدف از نوروپلیتیک، گردآوری و یکپارچهسازی نظریات و روشها به منظور بررسی مکانیسمهای شناختی عصبی در شناخت و رفتار سیاسی است. نوروساینس سیاسی دامنه وسیعی از علوم مانند نوروساینس، علوم سیاسی، روانشناسی، ژنتیکرفتاری، پریماتولوژی و الهیات را دربر میگیرد.در ادامه نتیجه یافتههای علمی شانزده مطالعه در جدول زیر ارائه شده است:

جدول زیر عملکرد مغزی لیبرالها و محافظهکاران را در سنین مختلف و همچنین گرایش های سیاسی دموکراتها و جمهوریخواهان نشان می دهد. 68% افراد انقلابی عملکرد مغزی محافظه کارانه را نمایش می دهند . 25% آزادیخواهان عملکر د مغزیشان محافظهکارانه است و 30% افراد مستقل عملکرد مغزی محافظه کارانه دارند.

با افزایش سن عملکرد مغزی محافظهکارانه افزایش مییابد. این موضوع از این نظر حائز اهمیت است که پیشبینی رفتار انتخاب کنندگان در انتخابات بستگی به اکثریت سنی شرکت کننده خواهد داشت. مثلا شاید قابل پیش بینی باشد زمانی که متولدین دهه 60 به سنین میانسالی برسند به دلیل جمعیت زیاد این دهه سنی تا بیست یا سی سال کشور ایران توسط افرادی با عملکرد مغزی محافظه کارانه اداره خواهد شد.
البته این تحقیقات در چند مورد، هنوز پاسخ روشنی ندارد. مثلاً این که افرادی که اصولا فاقد گرایش سیاسی هستند، عملکرد مغزیشان چگونه است؟ یا عملکرد مغزی تروریستها چگونه است؟ هر چند ظاهراً مطالعاتی در این خصوص در حال انجام است.
1.https://en.wikipedia.org/wiki/Neuropolitics
2.http://2012election.procon.org/view.resource.php?resourceID=004818
3. Michael D. Dodd, PhD, Amanda Balzer, PhD, Carly Jacobs, MA, Michael Gruszczynski, MA, Kevin B. Smith, PhD, and John R. Hibbing, PhD, "The Left Rolls with the Good; The Right Confronts the Bad. Physiology and Cognition in Politics," Philosophical Transactions of the Royal Society B: Biological Sciences, Mar. 5, 2012
4.Scott Eidelman, PhD, Christian S. Crandall, PhD, Jeffrey A. Goodman, PhD, and John C. Blanchar, "Low-Effort Thought Promotes Political Conservatism," Society for Personality and Social Psychology, 2012
5.Kevin B. Smith, PhD, Douglas Oxley, PhD, Matthew V. Hibbing, PhD, John R. Alford, PhD, and John R. Hibbing, PhD, "Disgust Sensitivity and the Neurophysiology of Left-Right Political Orientations," PLOS ONE, Oct. 19, 2011
6.Ryota Kanai, PhD, Tom Feilden, Colin Firth, and Geraint Rees, PhD, "Political Orientations Are Correlated with Brain Structure in Young Adults," Current Biology, Apr. 7, 2011
7.Erik G. Helzer and David A. Pizarro, PhD, "Dirty Liberals! Reminders of Physical Cleanliness Influence Moral and Political Attitudes," Psychological Science, Mar. 18, 2011
8.glas R. Oxley, PhD, Kevin B. Smith, PhD, John R. Alford, PhD, Matthew V. Hibbing, PhD, Jennifer L. Miller, Mario Scalora, PhD, Peter K. Hatemi, PhD, and John R. Hibbing, PhD, "Political Attitudes Vary with Physiological Traits," Science, Sep. 19, 2008
م
روش کردن ژن های خاموش شده
روشن کردن ژن های خاموش شده با استفاده از CRISPR/Cas9
محققین تکنیک جدیدی را با استفاده از CRISPR/Cas9برای روش کردن ژن های خاموش شده و تغییر سرنوشت سلول ها طراحی کرده اند.
به گزارش بنیان به نقل از medicalxpress، توانایی کنترل بیان ژن ها در سلول ها به محققین اجازه درک عملکرد و دستکاری سرنوشت سلول ها را می دهد. اخیرا، محققین یک روش انقلابی را در زمینه ویرایش ژن ایجاد کرده اند که CRISPR/Cas9 نام دارد. این روش به آن ها اجازه می دهد که به طور دقیق بخش های خاصی از DNA را به ژنوم اضافه کنند، بردارند و یا آن را جایگزین کنند. این روش کارآمدترین، ارزان ترین و آسان ترین ابزار موجود تا به امروز برای ویرایش ژن محسوب می شود. اما محققین هنوز نتوانسته اند به طور موثر از آن برای فعال سازی ژن ها استفاده کنند.
اما به تازگی تیمی از محققین ژاپنی در دانشگاه هوکاییدو روش قدرتمندی را برای رسیدن به این خواسته طراحی کرده اند. ژن ها درون سلول ها سوئیچ های مربوط به خودشان تحت عنوان پروموتور را دارند. زمانی این سوئیچ ها خاموش هستند که متیله باشند. محققین شدیدا خواستار روش کردن این ژن های خاموش شده هستند. آن ها یک مکانیسم ترمیم DNA به نام MMEJ را با CRISPR/Cas9 ترکیب کردند بطوریکه پروموتور متیله را با استفاده از CRISPR/Cas9 برش دادند و سپس یک پروموتور غیر متیله را با استفاده از MMEJ وارد کردند و در نتیجه یک سوئیچ خاموش را با یک سوئیچ روشن جایگزین کردند. آن ها این ابزار را روی یک ژن سلول عصبی به نام OLIG2 و ژن NANOG سلول های بنیادی جنینی تست کردند تا کارایی آن را در سلول های کشت شده بررسی کنند. ظرف پنج روز، آن ها شواهدی را یافتند که این ژن ها شدیدا بیان می شوند. مثلا در مورد روشن کردن OLIG2 در سلول های بنیادی انسانی کشت داده شده، سلول های با کارایی بسیار بالا ظرف مدت 7 روز به نورون تمایز یافتند. به نظر می رسد که این ابزار پتانسیل استفاده در دستکاری بیان ژن ها، ایجاد مدارهای ژنتیکی و یا مهندسی سرنوشت سلول ها را داشته باشد.
اندیشه کن
اندیشیدن را جدی بگیریم.
اندیشیدن به آنچه کم داریم. مردان و زنانی هستند که اندیشیدن را جدی گرفته باشند؟
اندیشیدن باید به مثابه یک کار مهم تلقی شود.
بند زبان را ببندیم و بال اندیشه را بگشاییم.
برای گفتن همیشه وقت هست ولی برای اندیشیدن ممکن است دیر شود.
به اندیشه مان بیندیشیم!
خوش درخشیدن در اندیشیدن است.
ژن درمانی
- امکان
دارد، ژن درمانی قادر به جبران کردن یک ژن جهش یافته سلولی که نوعی جهش از
دست دهنده عملکرد دارد، بکار برود. مثلا برای درمان بیماری مغلوب اتوزومی
فنیل کتونوریا.
 |
- گستردهترین کاربرد احتمالی ژن درمانی در رسیدن به اثری فارماکولوژیک، جهت مقابله با آثار یک ژن یا ژنهای جهش یافته سلولی یا مقابله با ایجاد بیماری به طریق دیگر باشد. مبتلایان به بیماری اکتسابی از جمله سرطان، از این روش بهره میبرند.
حداقل شرایط لازم برای ژن درمانی اختلال ژنتیکی
- شناسایی جایگاه ژنی درگیر یا حداقل اساس بیوشیمیایی آن اختلال.
- بار قابل توجه تبادل توجه بیماری و نسبت مطلوب خطر.
- داشتن فایده در مقایسه با درمانهای دیگر.
- آگاهی کافی از اساس مولکولی بیماری.
- اجزای تنظیم کننده مناسب برای ژن انتقال یافته.
- یک سلول هدف مناسب با نیمه عمر ترجیحا طولانی یا قابلیت همانندسازی خوب در داخل بدن.
- اطلاعات کافی از مطالعات سلولهای کشت داده شده.
خصوصیات ژن انتقال یافته
یک ژن انتقال یافته اکثرا از یک DNA مکمل تحت کنترل توالی پیشبری که ممکن است، لزوما پیشبر طبیعی ژن نباشد تشکیل شده است. عناصر تنظیم کننده باید طوری انتخاب شوند که ژن در سطوح کافی در سلولهای هدف رونویسی شود و در صورت لزوم به پیامهای تنظیم کننده ضروری پاسخ دهد.
خصوصیات سلول هدف
یکی از ملاحظات مهم در انتخاب سلول هدف مناسب این است که نیمه عمر طولانی در بدن یا قابلیت همانند سازی چشمگیر داشته باشد تا اثر زیستی انتقال ژن واجد دوام لازم باشد. سلولهای هدف ایدهآل، سلولهای بنیادی یا سلولهای اجدادی با قابلیت همانند سازی بالا میشوند که از آنها میتوان به سلولهای بنیادی مغز استخوان اشاره کرد. همچنین سلولهای آندوتلیال ممکن است اهداف بویژه مفیدی برای انتقال ژن باشند. زیرا دیوارههای عروق خونی را مفروش میکنند. سلول هدف باید پروتئینها یا لیگاندهای دیگر لازم برای فعالیت زیستی را نیز فراهم کند.
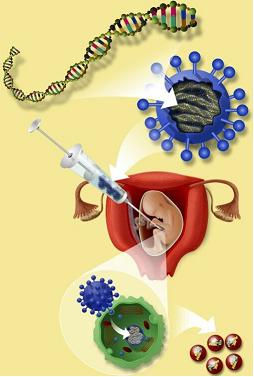 |
روشهای انتقال ژن
روش اول
وارد کردن ژن به داخل سلولهای کشت داده شده از بیمار در خارج بدن و سپس وارد کردن سلولها به بدن بیمار پس از انتقال ژن است.
روش دوم
روش دوم تزریق کردن مستقیم ژن به داخل بافت یا مایع خارج سلولی مورد نظر از طریق ناقلهای ویروسی و ناقلهای غیر ویروسی است. فناوری ناقلهای غیر ویروسی، هنوز در مراحل مقدماتی است.
ناقلهای ویروسی
ناقل ایدهآل برای ژن درمانی باید بیخطر باشد، به راحتی ساخته شود، به آسانی وارد بافت هدف گردد، بروز مادامالعمر ژن موردنظر در سطوح مناسب را فراهم کند. از انواع این ناقلها میتوان به رترو ویروسها و آدنوویروسها اشاره کرد. از مزایای ناقلهای ویروسی این است که قادرند وارد هر سلولی در جمعیت هدف شوند.
ناقلهای غیر ویروسی
اساسا جذاب هستند، زیرا فاقد مخاطرات زیستی (مانند آلودگی) مربوط به ناقلهای ویروسی هستند و تهیه آنها از نظر تئوری راحتتر است. این ناقلها 4 دسته هستند.
- DNA برهنه، مثلا DNA مکمل با عناصر تنظیم کننده در پلاسمید.
- DNA برهنه، بسته بندی شده در لیپوزمها.
- پروتئین که در آن DNA با پروتئینی مجموعه تشکیل میدهد و این پروتئین ورود مجموعه به داخل سلول یا بخشهای اجزای سلولی را تسهیل میکند.
- کروموزومهای مصنوعی.
 |
مخاطرات ژن درمانی
- بیمار میتواند واکنش نامطلوبی به ناقل یا ژن انتقال یافته بدهد.
- ژن انتقال یافته در DNA بیمار جای میگیرند و پروتوانکوژنی را فعال یا یک ژن سرکوب کننده تومور را غیر فعال میکند که موجب بدخیمی میشود.
- فعال شدن درجی میتواند انسجام یک ژن ضروری را از بین ببرند.
بیماریهای نامزد ژن درمانی
تعداد زیادی از اختلالات تک ژنی، نامزدهای بالقوه برای اصلاح از طریق ژن درمانی هستند. اینها شامل اختلالات خون سازی مانند تالاسمی، هموفیلی، انواع گوناگون کمبود ایمنی و نیز اختلالاتی مانند فنیل کتونوریا، کمبود α1- AT که هر یک بر پروتئینهایی که در کبد ساخته میشوند موثر هستند.
آینده بحث
تعداد زیادی کارآزمایی بالینی برای ارزیابی بیخطر بودن و کارآیی درمان با انتقال ژن در دست انجام است. نتایج اصلی میزگرد سال 1995 موسسه ملی سلامت در مورد وضعیت و آینده ژن درمانی هنوز صادق است. پیشرفت در این زمینه آهسته بوده. تاکید تحقیقات همواره مناسب نبوده و ادعاهای اولیه در مورد کارآیی آن مبالغه آمیز بوده است. با وجود این، میزگرد به این نتیجه رسید که ژن درمانی برای درمان بیماریهای انسانی در دراز مدت، بسیار امیدوار کننده است.